Аддитивные технологии создания многослойных аутотрансплантатов на основе клеточных продуктов в контролируемой среде
А.Н. СОЛОВЬЁВ1, М.Н. ШЕПЕТЬКО2, Н.М.ШЕПЕТЬКО3
1Учреждение образования «Белорусская государственная академия связи», ул. Ф. Скорины, 8/2, Минск, 220076, Беларусь
ORCID: https:// orcid.org/0000-0001-9675-6766
2Учреждение образования «Белорусский государственный медицнский университет», пр. Дзержинского, 83, г. Минск, 220083, Беларусь
ORCID: https:// orcid.org/0000-0002-6901-115X
3Учреждение здравоохранения «Городская клиническая больница скорой медицинской помощи», ул. Кижеватова 58, Минск, 220024, Беларусь
ORCID: https:// orcid.org/0009-0008-9784-3755
Поступила в редакцию 27 марта 2025
Обосновывается необходимость применения аддитивных технологий 3D печати живыми клетками реципиента для замещения аутотрансплантата кожи. Проводится анализ существующих устройств для обеспечения оптимальных параметров разрабатываемого 3D принтера. Приводится структурная схема 3D принтера для печати биочернилами в контролируемой стерильной среде.
Ключевые слова: аддитивные технологий, аутотрансплантат, 3D печать живыми клетками.
Введение. 3D-печать живыми клетками – это инновационная технология, которая позволяет создавать с помощью 3D-принтеров необходимый биологический материал либо органы. Эта технология имеет огромный потенциал в медицине, косметологии и смежных областях.
По оценкам Всемирной организации здравоохранения, ожоги представляют собой глобальную проблему, которая вызывает 265 000 смертей в год и являются одной из основных причин госпитализации детей в возрасте до 4 лет в мире [1]. В Республике Беларусь за медицинской помощью ежегодно обращается около 30 000 человек с термической травмой, среди которых более 15 % составляют дети. За 18 лет (2004 – 2021 гг.) в г. Минске по поводу ожогов и их последствий было госпитализировано более 18 тысяч детей. Наибольшее количество детей, требующих госпитализации по поводу ожогов, приходится на возраст от 0 до 3-х лет [2]. За 5 анализируемых лет (2018-2022 гг.) 207 детей были госпитализированы и находились на стационарном лечении в УЗ ГК БСМП г. Минска по поводу глубоких термических ожогов, которым для закрытия раневой поверхности была выполнена пластика свободным кожным лоскутом (аутодермопластика ожоговых ран) [3].
При наличии глубоких ожогов кожи (III Б – IV степени) требуется обязательное хирургическое восстановление кожного покрова [4]. В связи с тем, что ожоговая рана в большинстве случаев неоднородна по глубине, при обширных повреждениях наиболее рациональной тактикой является уменьшение площади ожоговой поверхности, путем максимального заживления поверхностных ожоговых ран. В процессе лечения, когда четко становятся видны границы поверхностного и глубокого ожога, диагноз уточняется и консервативные методы лечения уже направлены не на заживление, а на подготовку раневой поверхности к хирургическому лечению – аутодермопластика ожоговых ран [5].
Одной из самых интересных публикаций по исследованию значения клеточных технологий является публикация в журнале The Lancet за 2018 г, сделанная канадскими исследователями. Авторы обозначили целый ряд ключевых вопросов, касающихся ожоговой травмы, а именно: 1) быстрое заживление ожоговой раны есть самый главный фактор выживаемости и благоприятного прогноза; 2) обширная раневая ожоговая поверхность может превышать внутренние резервы организма и его репаративные способности к заживлению полученной раны; 3) несмотря на то, что аутотрансплантация в виде аутодермопластики является золотым хирургическим стандартом для лечения пациентов с большой площадью ожоговых ран, отсутствие неповрежденной кожи будет препятствием для успешной и полной аутотрансплантации при больших размерах ожоговой поверхности [6]. Характерные особенности лечения пациентов с большой площадью ожоговых ран: дефицит донорских ресурсов, необходимость выполнения нескольких аутодермопластик и неоднократное использование одних и тех же донорских мест после их заживления. Обширные раневые поверхности требуют большого количества хирургических операций. Аутодермопластика является основным способом закрытия ожоговых ран. Учитывая острую необходимость раннего закрытия ран на больших площадях у тяжело обожженных пациентов и в то же время дефицит донорских ресурсов, используются экономные методы кожной пластики («сетчатые» трансплантаты с заданным коэффициентом увеличения площади) [7].
В настоящее время одним из последних и перспективных направлений лечения ожогов может рассматриваться использование стволовых и собственных клеток кожи. Эта методика способствует не только заживлению поврежденного кожного покрова, но и восстановлению пигментации кожи, волос, сальных и потовых желез, иннервации, сосудистого сплетения и дермы [8].
Постоянное совершенствование методов лечения позволяет рассмотреть 3D-печать живыми клетками кожи как одну из перспективных технологий для применения в медицине. К основным направлениям применения биопринтеров можно отнести:
- трансплантацию кожи, так как пересадка аутотрансплантатов (аутологичная трансплантация – трансплантация самому себе) пациента требует достаточного объема подходящей кожи, что может быть ограничено обширной потерей кожи и дефицитом донорских участков [9], тогда 3D-печать кожи может использоваться для создания аутотрансплантатов для пациентов с ожогами, ранами или хроническими язвами;
- тестирование лекарств и косметики – искусственная кожа может использоваться для тестирования косметики и фармацевтических препаратов, что снижает необходимость в испытаниях на животных.
Разработка 3D печати различными материалами ведется достаточно давно и успешно. Комплектующие для производства 3D принтеров получили широкое распространение ввиду востребованности при конструировании и мелкосерийном производстве печатающих устройств. Различные производители закрывают практически все сегменты рынка по качеству и стоимости комплектующих под нужды заказчика, предоставляя разработчикам 3D принтеров широкий инструментарий для производства станка под конкретные нужды. Для управления используются открытые программные проекты, разрабатываемые международным сообществом для систем на микроконтроллерах, одноплатных компьютерах и специализированных платах c программируемой логической интегральной схемой [10]. Системы управления позволяют в достаточной мере использовать возможности проектируемых принтеров.
Определение решаемых задач и требований к оборудованию. Для биопринтеров в отличие от промышленных 3D принтеров существуют специфические требования ввиду выполнения особых задач по печати живыми клетками.
Основная задача на начальном этапе – выработка необходимых технических характеристик и получение структурной схемы образца биопринтера с возможностью печати тканей клеточным материалом для использования в научных исследованиях и клинического применения произведенного материала.
Основные отличия от печати пластиками заключаются в необходимости создания особой среды для работы с живыми культивируемыми клетками в области печати, которая должна обеспечивать стерильность, температурный режим с возможностью контроля водородного показателя (pH) [11].
Также к особенностям можно отнести работу с жидкими биочернилами и гидрогелями, которые печатаются в жесткую биорастворимую основу, что может требовать наличия нескольких экструдеров для различных материалов [12].
Работы клеточными материалами с наполнителями небольших размеров повышают требования к точности и контролю параметров печати для повышения выживаемости клеток при экструзии на оптимальной скорости печати.
Анализ существующих решений. Существующие решения представлены различными биопринтерами. В рамках данной статьи рассмотрим некоторые устройства, позволяющие печатать живые аналоги кожи из культивированных клеток пациентов.
Среди коммерческих производителей есть компании представляющие передовые устройства с хорошей поддержкой, среди них – Allevi, RegenHu и Cellink.
У перечисленных производителей можно найти по несколько моделей биопринтеров на официальных страницах в сети интернет. Особый интерес представляют принтеры с закрытой камерой, так как только в таких корпусах можно создать условия стерильности и намного проще соблюдать необходимые температурные режимы. Также к преимуществам можно отнести работу с несколькими экструдерами, у некоторых моделей количество экструдеров доходит до шести – Cellink Bio X6.
RegenHU представляют из себя конфигурируемые рабочие места c возможностью размещения до пяти печатающих экструдеров с возможностью раздельного контроля температуры, вакуумную систему крепления образцов, четыре различные рабочие зоны печати с возможностью контроля температуры, систему калибровки игл и подложек, систему фотофиксации печатаемых образцов [13]. Управляются коммерческие биопринтеры закрытым программным обеспечением, разработанным производителями под соответствующую модель.
При несомненных преимуществах перечисленные принтеры имеют довольно высокую цену, которая обусловлена наукоемким производством и необходимостью содержать высокотехнологичную компанию дорогостоящих специалистов.
Как альтернатива закрытым проектам существует несколько биопринтеров, разрабатываемых сообществом под свободной лицензией, например проект шприцевого насоса-экструдера, который можно загрузить в виде файла STL с http://3dprint.nih.gov/ и распечатать на любом 3D-принтере [14]
К преимуществам таких принтеров можно отнести низкую стоимость, широкую доступность компонентов и поддержку сообщества. Недостатком таких решений, как и прежде остаются низкая скорость исправления обнаруженных ошибок и зависимость проекта от бескорыстного интереса участников.
Разработка концепции биопринтера. Для реализации поставленных задач необходимо разработать концепцию биопринтера для печати живой кожи начиная от экструдера, механики, закрытого корпуса, системы управления с пользовательским интерфейсом и заканчивая тестированием и оптимизацией с учетом определенных задач и анализа существующих решений, чтобы собрать доступный биопринтер с необходимыми характеристиками.
Одним из ключевых элементов принтера является экструдер, так как его характеристики зачастую определяют остальные компоненты. При низкой производительности экструдера возникает вопрос необходимости использования быстрых приводов и лучше выбрать более точные с большим количеством шагов на оборот, а при относительно большом сопле, которое способно выдавать большой поток материала нет смысла гнаться за точностью в десятки раз превышающей диаметр выходного отверстия экструдера.
Для экструзии применяется несколько типов воздействия на биочернила в экструзионных принтерах:
- пневматическая экструзия (под давлением воздуха) – при такой экструзии используются электромагнитные клапаны, которые дозируют биочернила находящиеся под постоянным давлением. Такая экструзия характеризуется высокой разрешающей способностью, производительностью и довольно высокой выживаемостью клеток [15,16] однако слишком вязкие биочернила с большим количеством клеток могут забить сопло такого экструдера;
- механическая экструзия является одной из самых доступных, так как является производной от печати пластиком. При таком методе биочернила подаются с помощью актуатора или шагового двигателя посредством шнека. Такая экструзия позволяет работать с вязкими и жидкими материалами (при печати в емкость с гелем) [17] однако имеет низкую разрешающую способность (10-100 мкм) и выживаемость клеток в пределах 40-80% [18];
- струйные системы, первые применения которых упоминаются с использованием струйных принтеров [19], такие системы имеют очень высокое разрешение (пико литры) и высокое быстродействие, однако, как и при пневматической экструзии требуются биочернила низкой вязкости, кроме того, в таких принтерах присутствует эффект оседания клеток, что требует перемешивания материала перед печатью. Выживаемость клеток при таком методе остается высокой >85% [18] однако печать больших объемов остается слабым местом такого типа экструзии.
Для реализации опытного образца предлагается использовать механическую экструзию, которая является наиболее распространенной технологией и позволит получить результаты с наименьшими затратами при удовлетворительном качестве.
После выбора типа экструзии необходимо определиться с точностью позиционирования для выбора исполнительных механизмов. Опираясь на инструкцию по нанесению биочернил с клетками кожи [19] можно выделить то, что применяется сопло диаметром 500 мкм. Таким образом точность позиционирования для послойного создания сплошной области может быть выбрана в 100 мкм с пятикратным запасом.
Скорость печати должна быть определена в результате исследования на выживаемость клеток, так как при ускорении печати потребуется создавать большее давление для обеспечения потока, выбор оптимального показателя по выживаемости и скорости будет и будет искомым показателем, предварительно можно заложить скорость перемещения до 5 мм/с.
Для успешной печати как указывалось выше в закрытой камере должны соблюдаться определенные условия, позволяющие развиваться клеткам, к таким условиям можно отнести:
- поддержание необходимой температуры и влажности;
- возможность печати в гели и жидкости;
- использование материалов, устойчивых к стерилизующим средствам;
- системы УФ-стерилизации или антимикробные покрытия;
- системы фильтрации воздуха с нагнетанием для создания барьера от окружающей среды.
Структурная схема. С учетом вышеуказанных особенностей была разработана структурная схема биопринтера для печати клеточным материалом представленная на рис. 1.
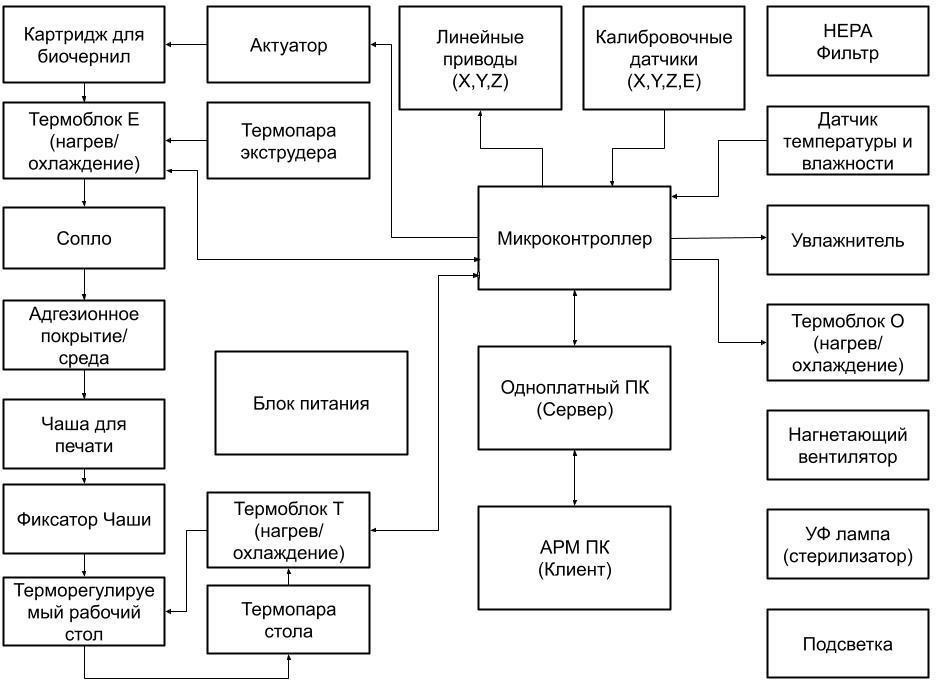
Рис. 1. Структурная схема биопринтера
Перед началом работы для частичного обеспложивания рабочей зоны включается ультрафиолетовая (УФ) лампа, что, однако не приводит к полной стерилизации воздуха в области печати.
HEPA фильтр предназначен для механической стерилизации и поддержания стерильности в процессе печати [20], очищения от вирусов, бактерий и частиц поступающего в нагнетающий вентилятор воздуха.
Нагнетающий вентилятор создает внутри корпуса избыточное давление, которое не позволяет мелким частицам попадать внутрь корпуса и загрязнять печатающиеся образцы.
Для отслеживания условий печати в корпусе расположен датчик температуры и влажности, данные с которого поступают на микроконтроллер (МК), МК может корректировать внутренние условия в закрытом корпусе управляя Термоблоком О и увлажнителем для достижения необходимых показателей температуры и влажности. Термоблоки должны обеспечивать не только нагрев, но и охлаждение для печати специфическими материалами [21].
При необходимости и недостаточном освещении можно использовать встроенную подсветку. После начальных процедур можно приступать к установке картриджа с биочернилами, управление экструзией осуществляется актуатором, которым управляет МК регулируя давление согласно программе печати.
Для контроля температуры в зоне экструдера применяется термопара экструдера, по сигналу, поступающему с термопары термоблок регулирует заданную температуру удерживая ее в заданных МК рамках, термоблоки также следят за работоспособностью и должны сигнализировать о нештатных и аварийных ситуациях в зонах ответственности. Термоблоки могут быть программными функциями, выполняемыми МК или одноплатным ПК
Для обеспечения точности печати в принтере должны быть предусмотрены калибровочные датчики (X, Y, Z, E), которые проверяют положение осей и экструдера, они могут быть как физические, так и программные, основанные на показаниях тока на шаговых двигателях, которые срабатывают при превышении рабочего тока исполнительного устройства, вызванного механическим ограничителем движения по оси.
Фиксатор чаши должен надежно закреплять чашу для печати на платформе механически или с помощью магнитов.
Печать осуществляется по следующему алгоритму, разработанная модель подготавливается на автоматизированном рабочем месте (АРМ) на ПК со специализированным программным обеспечением (ПО). После чего файл с инструкциями передается на исполнение в одноплатный ПК и дальнейший контроль процесса осуществляется именно на нем.
АРМ предоставляет пользовательский интерфейс для управления процессом печати, ход которой можно наблюдать в браузере, отслеживать ошибки и отправлять команды на коррекцию печати при необходимости.
МК, получая команды от одноплатного ПК занимается управлением линейными приводами (X, Y, Z), которые перемещают экструдер согласно командам, и отслеживанием датчиков, экономя вычислительные ресурсы, что существенно поднимает быстродействие всей системы.
Адгезионное покрытие/среда обеспечивает прилипание первого слоя к платформе или фиксацию в пространстве, если печать идет в жидкой гелеобразной среде.
Термоблок E поддерживает оптимальную температуру чернил, а термопара экструдера отслеживает ее для поддержания необходимого режима работы
Терморегулируемый рабочий стол и термопара стола контролируют температуру для предотвращения деформации и поддержания необходимой температуры печатной среды.
После завершения печати термоблок O может использоваться для отверждения или стабилизации напечатанной структуры, а одноплатный ПК сохраняет данные о печати и отправляет отчет на АРМ ПК.
Представленная структурная схема может быть упрощена при необходимости экономии, либо расширена функциями отслеживания и компенсации вибрации при необходимости увеличения скорости печати, а также функцией удаленного мониторинга посредством Web камеры.
Заключение. Биопринтер разработанный по приведенной структурной схеме может быть использован для качественной печати кожи живыми клетками. На следующих этапах предполагается осуществить подбор комплектующих, разработать дизайн и конструкцию корпуса, подобрать необходимое программное и электронное обеспечение, провести тесты и напечатать опытные образцы для дальнейшей оптимизации печати учитывая критерии выживаемости клеток и скорости печати.
При разработке следует рассмотреть ассортимент предлагаемых картриджей с биочернилами для определения возможности использования наиболее доступных материалов, либо рассмотреть возможность создания собственных материалов для печати.
ADDITIVE TECHNOLOGIES FOR CREATING MULTILAYER AUTOTRANSPLANTS BASED ON CELL PRODUCTS IN A CONTROLLED ENVIRONMENT
A.N. SALAUYOU, M.N. SHAPETSKA, N.M. SHAPETSKA
Abstract
The necessity of using additive technologies of 3D printing with living cells of the recipient for replacement of autotransplant of skin is substantiated. The analysis of existing devices is conducted to provide optimal parameters of the developed 3D printer. The structural diagram of the 3D printer for printing with bioinks in a controlled sterile environment is given.
Список литературы
- World Health A WHO plan for burn prevention and care. – Geneva : WHO, 2008. – 23 p.
- Шепетько, Н. М. Анализ детской ожоговой травмы в г. Минске за период 2004–2021 гг. / Н. М. Шепетько, Е. В. Дюбченко, Ю. А. Драер // Здравоохранение. – 2022. – № 10. – С. 17–23.
- Шепетько, Н. М. Диагностические сложности при оценке ожоговой травмы у детей на различных этапах оказания медицинской помощи / Н. М. Шепетько // Здравоохранение. – 2024. – № 1. – С. 44–51.
- Часнойть, А. Ч. Эффективность лечения ожоговой травмы на модели сплошного и мозаичного ожогов у животных с использованием тканевого эквивалента кожи / А. Ч. Часнойть [и др.] // Медицинский журнал. – 2022. – № 3(81). – С. 24–29.
- Кошельков, Я. Я. Избранные лекции по «Комбустиологии и криопатологии» : учеб. пособие / Я. Я. Кошельков, А. Е. Серебряков. – Минск : БелМАПО, 2012. – 120 с.
- Amini-Nik, S. Stem cells derived from burned skin – the future of burn care / S. Amini-Nik [et al.] // EBioMedicine. – 2018. – Vol. 37. – P. 509–520.
- Жилинский, Е. В. Анализ летальности, основных прогностических факторов и осложнений среди пациентов с ожоговой травмой / Е. В. Жилинский, А. Ч. Часнойть, С. А. Алексеев // Мед. новости. – –№ 11. – С. 87–91.
- Соболева, М. Ю. Морфофункциональные особенности восстановления целостности кожи при термической травме / М. Ю. Соболева // Клиническая и экспериментальная морфология. – – Т. 8, № 1. – С. 71–77.
- Смирнов, С. В. Инновационные технологии местного лечения ожогов в НИИ СП им. Н.В. Склифосовского / С. В. Смирнов, В. Б. Хватов // Новая экономика. Инновационный портрет России. – М. : Центр стратегического партнерства, 2009. – С. 388–390.
- Балгуданян, И. А. Разработка 3D-принтера на основе системы на кристалле с ПЛИС / И. А. Балгуданян [и др.] // Системный администратор. – 2020. – № 6. – С. 44–49.
- Колокольцова, Т. Д. Современные способы выделения и культивирования клеток человека и животных : учеб. пособие / Т. Д. Колокольцова, И. Н. Сабурина, А. А. Кубатиев. – М. : ФГБОУ ДПО РМАНПО, 2016. – 50 с.
- 3D Bioprinting Solutions: R-GEN 200 3D Bioprinter [Electronic resource]. – Mode of access : https://www.regenhu.com/3dbioprinting-solutions/r-gen-200-3dbioprinter/#comprehensive-instrument- control. – Date of access : 10.01.2024.
- Hinton, T. J. Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels / T. J. Hinton [et al.] // Science Advances. – 2015. – Vol. 1, Iss. 9.
- Ng, W. L. Microvalve-based bioprinting – process, bio-inks and applications / W. L. Ng [et al.] // Biomaterials Science. – 2017. – Vol. 5. – P. 1–15.
- Horváth, Engineering an in vitro air-blood barrier by 3D bioprinting / L. Horváth [et al.] // Scientific Reports. – 2015. – Vol. 5, № 1. – P. 7974.
- Hinton, T. J. Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels / Hinton T.J. [et al.] // Science Advances. – 2015. – Vol. 1. – P. 1–10.
- Волотовский, И. Д. Трехмерная 3D-биопечать: основы технологии и ее использование в интересах биологии и медицины / И. Д. Волотовский, С. В. Пинчук // Институт биофизики и клеточной инженерии НАН Беларуси. – Минск, Республика Беларусь. – 2022. – Т. 67, № 1. – С. 114–126.
- Roth, E. A. Inkjet printing for high throughput cell patterning / E. A. Roth [et al.] // Biomaterials. – 2004. – Vol. 25. – P. 3707–3715.
- Jorgensen, M. Multicellular bioprinted skin facilitates human-like skin architecture in vivo /
- M. Jorgensen [et al.] // Science Translational Medicine. – 2023. – Vol. 15. – Iss. 716.
- Борисов, Л. Б. Медицинская микробиология, вирусология и иммунология / Л. Б. Борисов. – М. : МИА, 2005. – 156 с.
- Xu, L. Bioprinting a skin patch with dual-crosslinked gelatin (GelMA) and silk fibroin (SilMA): An approach to accelerating cutaneous wound healing / L. Xu [et al.] // Materials Today Bio. – 2023. – Vol. 18.















